Ayrışma Tepkimeleri
Analiz Tepkimesi Nedir, Örnekleri Nelerdir?
Kütle spektrometresi
Gravimetrik analiz ve termogravimetrik analiz için kullanılabilmektedir.
Rekasiyon, gerçekleşen tepkimeye verilen isimdir. Reaktif ise tepkimeye giren bileşik olarak ifade edilmektedir.
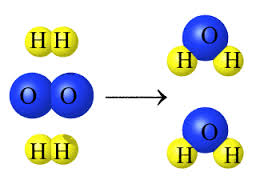
Ayrışma reaksiyonlarında; su elektroliz yolu ile hidrojen ve oksijene ayrışmaktadır.
2H2O --> 2H2 + O2
Potasyum klorat, potasyum klorür ile oksijene ayrışabilir.
2 KClO3 ---> 2 KCl + 3 O2 şeklindedir.
Diğer örnekler ise;
NH3 --> N2 + H2
2NaHCO3 ---> Na2CO3 + CO2 + H2O
LiClO3 ---> LiCl + O2
C6H12O6 ---> 2C2H5OH + 2CO2
H3PO4 ---> P2O5 + H2O
NaOH ---> Na2O + H2O
HNO3 ---> N2O5 + H2O şeklindedir.
Analiz tepkimelerinde bir maddeden çok daha fazla madde elde edilmektedir. Sentez tepkimelerinde ise birden fazla madde tepkimeye girip bir tane madde oluşturulmaktadır. Analiz tepkimelerinin tam tersi sentez tepkimeleri olarak ifade edilmektedir. Sentez tepkimelerinin tersi ise analiz tepkimesi olarak ifade edilmektedir.
Bu tepkimelerde elektron alış verişi sonucu atomların değerlikleri değişir. Yanma tepkimeleri, elementlerinden oluşum ve elementlerine ayrışma tepkimeleri, tek yer değiştirme tepkimeleri, aynı zamanda redoks tepkimesidir.
CH4(g) + 2O2(g) ===> CO2(g) + 2H2O(g)
Tepkimesi, metanın yanma tepkimesidir. Bu tepkimede O2 nin değerliği sıfır, metandaki karbonun -4, hidrojenin +1’dir. Tepkime sonunda CO2 deki karbonun değerliği +4, CO2 ve H2O’daki oksijenin değerliği, -2 dir. Kısacası tepkimede metan karbonu yükseltgenmiş (electron vermiş), oksjien ise indirgenmiştir (elektron almış).
N2(g) + 3H2(g) ===> 2NH3(g)
Tepkimesi, amonyak bileşiğinin elementlerinden oluşumunu;
2H2O(s) ===>2H2(g) + O2(g)
tepkimesi, suyun elementlerine ayrışmasını gösteren tepkimelerdir ve bu tepkimelerde de atomların değerlikleri değişmektedir.
Zn (k) + CuSO4 (aq) ===> ZnSO4(aq) + Cu(k)
Tepkimesi tek yer değiştirmeye örnektir (Asit-baz tepkimeleri ve çökelme tepkimeleri ise çift yer değiştirmeye örnek oluşturur).
Bunu beğen:
BeğenYükleniyor...